Ultrahohe Magnetfelder in der Magnetresonanz-Bildgebung: Lohnt es sich?
Forschungsbericht (importiert) 2010 - Cyberneum
Die Magnetresonanztomographie (MRT) ist ein Verfahren, das in der klinischen Diagnostik ebenso wie in der biologischen und neurowissenschaftlichen Grundlagenforschung in immer noch steigendem Maße Anwendung findet. Es basiert auf den speziellen Eigenschaften vieler Atomkerne in einem starken Magnetfeld und erlaubt Einblicke in die Struktur und Funktion innerer Organe, ohne die schädlichen Wirkungen, die bei Röntgenstrahlen oder Radioaktivität auftreten. Über die reine Darstellung der Anatomie hinaus erlaubt die Vielseitigkeit dieser Technik ihren Einsatz in zahlreichen Untersuchungsbereichen, etwa zur quantitativen räumlichen Messung der Organdurchblutung, zur Darstellung von Faserverläufen durch Messung der Diffusion oder zur Erkennung von Gehirnaktivität in der funktionellen Bildgebung. Gerade die letztgenannte Technik gehört inzwischen zu den wichtigsten Instrumenten der Gehirnforschung, wie durch die häufige Berichterstattung über gewonnene Erkenntnisse in den Medien gezeigt wird. Das zentrale Element eines MR-Tomographen ist ein Magnet, der ein starkes, aber auch sehr homogenes Magnetfeld erzeugt, wobei eine deutliche Tendenz zu steigenden Feldstärken zu beobachten ist. Übliche klinische Geräte haben Feldstärken zwischen 1,5 Tesla (T) und 3 T. Die MR-Tomographen am Magnetresonanzzentrum des Max-Planck-Instituts für biologische Kybernetik haben dagegen Felder von 9,4 T für Messungen am Menschen und 16,4 T für Studien an kleinen Tieren. In Anbetracht der großen Erfolge der konventionellen MR-Bildgebung stellt sich die Frage, ob diese immer höheren Feldstärken wirklich benötigt werden.
Wieso eigentlich Ultrahochfeld?
Trotz aller Erfolge, die die Magnetresonanztomographie sowohl in der klinischen als auch in der wissenschaftlichen Anwendung zeigt, hat sie doch auch eine fundamentale Einschränkung, nämlich ihre geringe Empfindlichkeit und die damit stark eingeschränkte räumliche Auflösung. Der Grund dafür liegt in den physikalischen Grundlagen der Magnetresonanz, die ausnutzt, dass viele Atomkerne in einem Magnetfeld unterschiedliche Energieniveaus einnehmen können. So haben die am meisten beobachteten Wasserstoffkerne zwei Energieniveaus, die zwei verschiedenen Zuständen einer Eigenschaft entsprechen, die Kernspin genannt wird. Die Magnetresonanztomographie beruht nun darauf, dass sich mehr Kerne in dem Zustand mit niedrigerer Energie befinden. Allerdings ist dieser Unterschied gering: Bei einem Feld von 3 T sind von einer Million Wasserstoffkernen nur etwa fünf Kerne mehr in dem niedrigeren Energiezustand als in dem hohen. Nur diese Kerne tragen aber zum Signal bei. Ein MR-Bild ist deshalb nur aufgrund der hohen Gesamtzahl von Wasserstoffkernen möglich. Der Besetzungszahl-Unterschied wächst aber mit steigendem Magnetfeld, sodass bei einer Feldstärke von 9,4 T immerhin schon 33, bei 16,4 T sogar fast 58 Atomkerne zum Signal beitragen.
Der Einsatz von hohen Magnetfeldern in der MRT soll somit vor allem zu einer Signalsteigerung führen – im Einsatz am Menschen wird ein etwa linearer Anstieg des Signals mit dem Magnetfeld erwartet, für Versuche an kleinen Tieren kann der Gewinn sogar deutlich größer ausfallen.
Neue Kontrastmechanismen
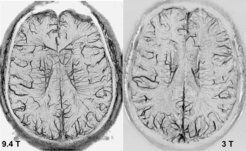
Für manche Anwendungen ist aber eine noch höhere Signalsteigerung möglich: Vor allem der Effekt von Unterschieden in den magnetischen Eigenschaften der Gewebe kann zu deutlichen Kontrasten führen, die mit klassischen Methoden nicht erreichbar sind. Ein Beispiel für solche Unterschiede der magnetischen Suszeptibilität, also der Wirkung auf das äußere Magnetfeld, bietet das Blut: Arterielles Blut ähnelt in seinen magnetischen Eigenschaften dem umliegenden Gewebe und ist deshalb nur schlecht zu identifizieren. Das im venösen Blut enthaltene deoxygenierte Hämoglobin ist aber paramagnetisch, das heißt, es beeinflusst das äußere Magnetfeld und führt dazu, dass das Signal aus den Venen schneller abklingt als im umgebenden Gewebe – die Venen werden dunkel. Da dieser Effekt stark mit der Magnetfeldstärke steigt, ist hier eine besonders hohe Verbesserung durch den Einsatz von Ultrahochfeld-Tomographen zu erwarten [1]. Ein Vergleich von Bildern, die mithilfe dieser Technik bei 3 T und 9.4 T aufgenommen wurden, zeigt eindrucksvoll die deutliche Steigerung in der Zahl der erkennbaren Gefäße (Abb. 1).
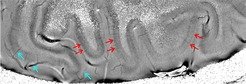
Doch nicht nur das deoxygenierte Blut in den Venen kann aufgrund seiner magnetischen Eigenschaften im MR-Bild dargestellt werden; etliche andere Effekte sind bekannt, die zu einer Änderung der magnetischen Suszeptibilität und damit zu einer Verzerrung des Magnetfeldes führen. So besteht eine Abhängigkeit von der Orientierung von Fasern [2], die die einfache Identifizierung von Nervenbündeln erlaubt, oder dem Austausch von Wasser mit Makromolekülen [3]. Vor allem sorgt aber auch der Eisengehalt des Gewebes für eine starke Änderung der magnetischen Eigenschaften. Strukturen mit hohem Eisengehalt sind somit gut zu erkennen. Dazu gehören einige Bereiche im Gehirninneren, vor allem aber auch sehr dünne Streifen innerhalb der Hirnrinde (Cortex), die nur aufgrund der Kombination aus hoher erreichbarer räumlicher Auflösung und gesteigerter Empfindlichkeit gegenüber Feldvariationen erkennbar sind (Abb. 2). Erstmals ist damit auch mit der MRI (Magnetic Resonance Imaging) die Darstellung intracortikaler Strukturen möglich [4]. Nicht zuletzt soll auch die funktionelle MRI vom Einsatz von Hochfeld-Magneten profitieren, da sowohl die Empfindlichkeit als auch die räumliche Spezifität mit steigendem Feld deutlich anwächst.
MR-Spektroskopie - ein Einblick in den Metabolismus
Ein weiteres Gebiet, in dem der Einsatz von hohen Magnetfeldern zu deutlichen Verbesserungen führt, ist die Untersuchung des Zellmetabolismus mittels der In-vivo-MR-Spektroskopie. Diese Technik erlaubt die Unterscheidung und Quantifizierung von verschiedenen Substanzen im Gehirn, ohne die Notwendigkeit, Proben zu entnehmen (Abb. 3).

Aufgrund der geringen Konzentration dieser Metaboliten ist die Empfindlichkeit hier ein entscheidendes Problem. Somit ist die Signalsteigerung durch die Ultrahochfeld-MR von besonderer Bedeutung. Zusätzlich werden die dicht gedrängten und sich überlappenden Spektrallinien in der Protonenspektroskopie mit steigender Feldstärke auseinandergezogen, was die quantitative Auswertung erleichtert. Bei einer Feldstärke von 16,4 T ist es damit in klinischen Studien möglich, bis zu 20 Substanzen aus einem relativ kleinen Bereich des Gehirns einer Ratte mit hoher Genauigkeit quantitativ zu bestimmen [5]. Zu den beobachteten Metaboliten gehören unter anderem Neurotransmitter (Glutamat, GABA, Glyzin) oder Substanzen, die für den Energiehaushalt der Zelle erforderlich sind (Creatin, Phosphorcreatin, Laktat, Glukose).
Um welchen Preis? Probleme der Ultrahochfeld-Magnetresonanz
Die großen Vorteile der Ultrahochfeld-Magnetresonanz sind aber nicht selbstverständlich: Änderungen in den Eigenschaften der benötigten Signale erfordern die Entwicklung neuer Technologien, um hochqualitative Ergebnisse zu erhalten. Das betrifft vor allem das Hochfrequenz-Feld, das verwendet wird, um die Atomkerne durch Anregung zur Signalabgabe zu bewegen. Während die Wellenlänge dieser Signale bei 1,5 T noch deutlich über einem halben Meter liegt, ist sie bei 9,4 T mit etwa 10 cm schon unterhalb der Größe des Gehirns. Das führt dazu, dass Welleneffekte, also die Überlagerung positiver und negativer Wellenteile auftreten, die bewirken, dass Teile des Objekts nicht angeregt werden und somit starke Intensitätsschwankungen über das Bild, bis hin zur vollständigen Signalauslöschung, auftreten (Abb. 4).
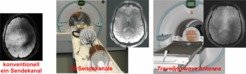
Neuartige Sendestrategien sind erforderlich, um trotz dieser Probleme homogene Bilder zu erhalten. So kann eine Gruppe von Antennen um das Objekt herum angebracht werden, die unabhängig voneinander zur Anregung beitragen. Durch einzelne Optimierung ihrer Signale kann das resultierende Gesamtfeld so eingestellt werden, dass innerhalb eines gewünschten Bereichs keine destruktiven Interferenzen auftreten. Das ermöglicht eine optimierte Abstimmung auf das einzelne Experiment, erfordert aber sowohl von der technischen als auch der methodischen Seite intensive Entwicklungen, da die Technologie der Mehrkanal-Sendespulen mit der dazugehörigen Steuerung aufwändig ist und Techniken zur schnellen Optimierung der Signale benötigt werden. Eine deutlich einfachere Methode, um ein akzeptables Sendefeld zu erreichen, besteht in dem neuartigen Ansatz des traveling wave imaging [6]: Hier wird mithilfe einer einfachen Antenne ein zirkular polarisiertes Feld erzeugt, das aufgrund seiner geringen Wellenlänge fast verlustfrei durch die Röhre des Magneten läuft. Das dabei im Gehirn entstehende Anregungsprofil ist hier automatisch relativ homogen. Diese Technik erlaubt zwar keine optimale Justierung des Signals auf den beobachteten Bereich, hat aber Vorteile durch den geringen Aufwand, mit dem eine oft ausreichende Homogenität erreicht werden kann.
Ausblick
Die Ultrahochfeld-MR-Bildgebung ist ein relativ neues Gebiet, in dem noch deutliche Entwicklungsleistungen erforderlich sind, bevor ihr volles Potenzial in der medizinischen und neurowissenschaftlichen Anwendung genutzt werden kann. Erste Ergebnisse zeigen allerdings auch jetzt schon, dass deutliche Steigerungen in der räumlichen Auflösung, in der Bildqualität und in der Genauigkeit quantitativer Messungen zu erwarten sind. Über die hier vorgestellten Beispiele hinaus sind aufgrund der veränderten Eigenschaften im hohen Magnetfeld in weiteren Gebieten große Verbesserungen zu erwarten, etwa in der Messung der Gehirndurchblutung, der Angiographie oder der Beobachtung von anderen Kernen als dem Wasserstoff.



